Définition d’une cellule souche
Les cellules souches sont des cellules qui ont la capacité unique à se multiplier et à se transformer – se différencier- en d’autres types de cellules. Tous les autres types de cellules du corps sont des cellules dites somatiques et différenciées, car elles ont chacune un rôle défini et précis à jouer et ne peuvent pas se transformer. Quelques exemples, le rôle d’une cellule cardiaque est de se contracter. Le rôle d’une cellule pancréatique est de produire de l’insuline. Une cellule gustative identifie les saveurs présentes dans les aliments. Une cellule intestinale absorbe les nutriments pour que ceux-ci soient disponibles dans les tissus. Les cellules souches sont situées majoritairement dans la moelle osseuse et n’ont pas d’autre rôle que de se transformer en d’autres types de cellules.
Le rôle naturel des cellules souches
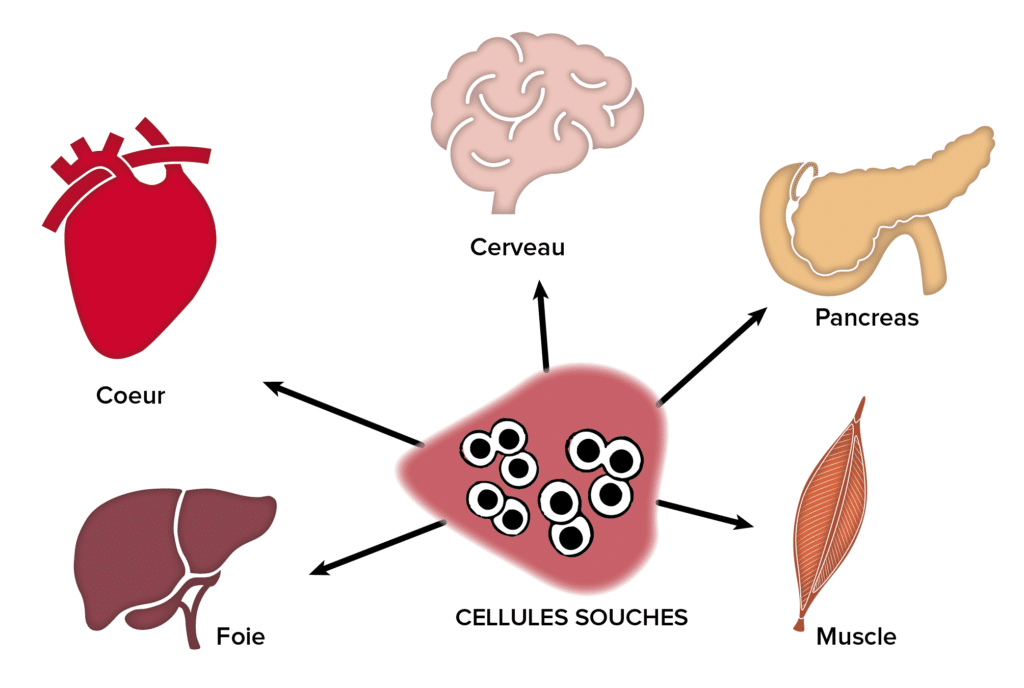
Au début des années 2000, des chercheurs avaient observé que des cellules souches du sang avaient la capacité de migrer au niveau du cerveau et de devenir des cellules du cerveau (Mezey E. et al., 2000). À la même époque, des observations similaires émergeaient, révélant que des cellules souches du sang avaient aussi la capacité de migrer au niveau du cœur et de devenir des cellules cardiaques (Orlic D. et al., 2001) ou au niveau du foie pour devenir des cellules hépatiques (Jang Y.Y. et al., 2004). La science traditionnelle des cellules souches adultes admettait à l’époque que les cellules souches de la moelle osseuse avaient la capacité de se transformer en cellules du sang strictement, étant les précurseurs des globules rouges, des globules blancs et des plaquettes sanguines. L’idée communément admise était qu’elles n’avaient pas la capacité de se transformer en d’autres types cellulaires. Donc, ces observations étaient novatrices et en contradiction avec les connaissances de l’époque. Sur la base de ces données et d’autres données disponibles à l’époque, l’hypothèse publiée (Jensen G et Drapeau C, 2002) était que les cellules souches de la moelle osseuse pouvaient se transformer en pratiquement n’importe quelle cellule du corps et donc constituaient le système naturel de réparation du corps humain (figure 1). Cette hypothèse est devenue au fil des années, grâce à plusieurs centaines d’articles publiés soutenant fortement cette hypothèse, un fait établi (pour revue, Drapeau C., 2010 ; Drapeau C. et al., 2012).
Figure 1 : les cellules souches de la moelle osseuse peuvent se transformer en pratiquement n’importe quelle cellule du corps. Elles constituent le système naturel de réparation du corps humain
Notre système naturel de réparation du corps : comment fonctionne-t-il ?
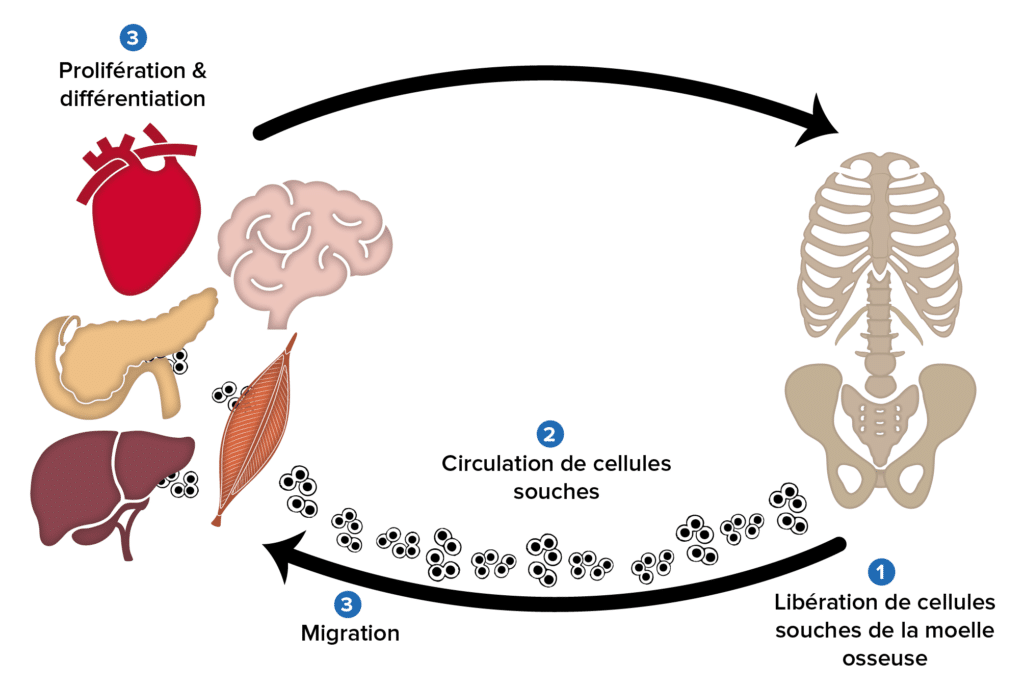
Chaque fois qu’une blessure ou une lésion au sein d’un tissu apparaît, celui-ci va libérer une première série de composés spécifiques, comme le G-CSF*. Ces molécules « signal » d’aide vont circuler migrer vers la moelle osseuse puis déclencher la libération de cellules souches de la moelle osseuse (figure 2). Durant les quelques jours qui suivent, une augmentation importante du nombre de cellules souches en circulation peut être observée. Ces cellules souches qui sont en circulation au niveau du sang ne savent pas quel est le tissu qui a fait appel à cette assistance (figure 2). Pour pouvoir identifier le tissu vers lequel elles doivent migrer, le tissu affecté, quelques jours après l’incident, va libérer une seconde génération de composés, comme le SDF-1**. Cette molécule de guidage va attirer et guider localement les cellules souches vers le tissu en besoin. Lorsqu’elles circulent dans les fins vaisseaux du tissu affecté, au contact de ces molécules de guidage, les cellules souches vont migrer dans le tissu affecté et au contact de débris cellulaires, elles vont se multiplier et se transformer en cellules du tissu local (figure 2). C’est par ce mécanisme que les cellules souches constituent le système de réparation naturel du corps humain (Drapeau C. et al., 2012).
Les cellules souches répondent ainsi aux 5 critères de définition d’un système. Un système du corps humain :
- Est formé de tissus ou d’organes
- Composé de cellules spécifiques
- Qui agissent sur d’autres tissus et organes
- Via une signalisation/un mécanisme d’action spécifique
- En vue de favoriser un bon état de santé et la survie de l’organisme entier
Le système naturel de réparation du corps humain est composé de cellules spécifiques, les cellules souches adultes, provenant majoritairement de la moelle osseuse, qui agissent sur d’autres tissus en étant mobilisées par des composés spécifiques (Leone et al., 2006) -, et en migrant à travers le tissu lésé, guidé par une seconde génération de composé spécifique (Swenson et al., 2008), puis en se multipliant et en se différenciant en tissu local. Ce mécanisme de réparation permet le renouvellement des tissus et organes du corps, en vue de maintenir la santé de l’organisme entier.
*G-CSF : Granulocyte Colony-Stimulating Factor
** SDF-1 : Stromal Cell-Derived Factor -1
Figure 2 : les différentes étapes permettant aux cellules souches de réparer les tissus en besoin. Suite à une blessure, le tissu lésé libère des composés déclenchant la libération des cellules souches de la moelle osseuse, qui vont circuler dans le sang pour y être distribuées au tissu en suivant des molécules de guidage produites par le tissu lésé. La cellule souche va migrer dans le tissu, se multiplier puis se différencier en tissu local.
Augmenter le nombre de cellules souches en circulation, une nouvelle approche thérapeutique
L’aspect qui a été le plus étudié est le nombre de cellules souches en circulation. À blessure égale, les personnes présentant plus de cellules souches en circulation ont une meilleure capacité de réparation démontrée par exemple suite à un AVC ou une fréquence d’événements cardio-vasculaires plus faibles (Werner et al., 2005; Tsai et al., 2014). En effet, avoir plus de cellules souches en circulation signifie avoir plus de cellules souches disponibles pour la réparation des tissus.
Donc suite à ces observations, le prélèvement de cellules souches d’un malade puis la réinjection de ces cellules ont démarré. La démarche a pour but d’augmenter le nombre de cellules souches en circulation. Après l’isolation des cellules souches de différentes sources, elles sont multipliées en laboratoire, puis réinjectées au patient. Une autre démarche plus physiologique consiste donc à augmenter la libération de nos propres cellules souches, nommée la mobilisation des cellules souches de la moelle osseuse. En augmentant le nombre de cellules souches en circulation, la capacité de ces différents tissus à se réparer est optimisée. L’évaluation de cette démarche a généré la publication de centaines d’articles scientifiques révélant le bénéfice d’augmenter le nombre de cellules souches en circulation dans le processus de réparation des tissus. Ces observations ont été réalisées sur une variété d’organes, comme par exemple le cœur (Leone et al., 2006 ; Orlic et al., 2001), ou le pancréas (Voltarelli et al., 2007); (revue Drapeau et al., 2012).
Les cellules souches sont responsables au quotidien du renouvellement des tissus
À travers ces études, il est essentiel de noter cette observation. Le processus de réparation, c’est-à-dire celui décrit précédemment à savoir, un tissu affecté faisant appel à la libération de cellules souches qui sont ensuite guidées vers le tissu pour le réparer, ce phénomène se déroule tous les jours en quantité plus faible en l’absence de blessure, afin de renouveler les tissus. En effet, chaque organe et tissu se renouvelle à des vitesses différentes. Par exemple, l’intestin se renouvelle en 3-5 jours, le pancréas et le cœur en plusieurs années. Ainsi chaque jour, dû au vieillissement cellulaire et à de nombreux facteurs, des cellules abîmées, altérées ont besoin d’être remplacées par de nouvelles cellules. Ce renouvellement est également effectué par les cellules souches qui tous les jours sont libérées de la moelle osseuse et circulent dans le sang, migrant vers le tissu selon les besoins.
Vers une nouvelle définition du « maintien de la santé »
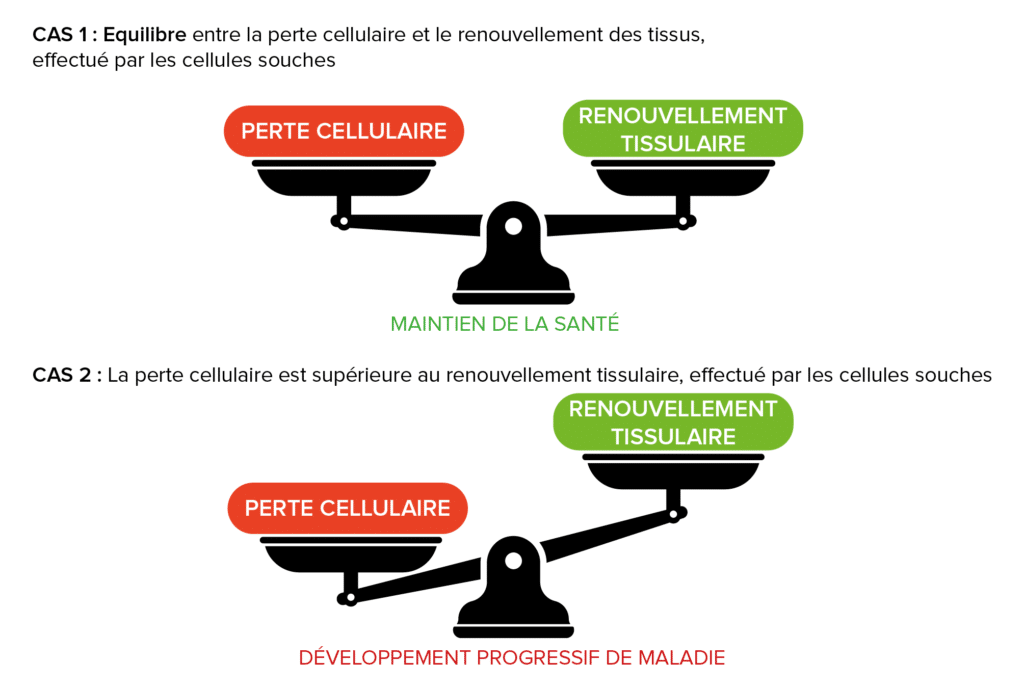
Cette nouvelle fonction des cellules souches génère ainsi une nouvelle définition du maintien en santé. Celle-ci serait en fait en partie un équilibre entre deux phénomènes qui se déroulent en continu au sein de notre organisme, la perte quotidienne de cellules d’un tissu, en parallèle de son renouvellement. Pour maintenir les tissus, le remplacement des cellules doit s’effectuer au même rythme que la perte cellulaire (figure 3 : cas 1). Si la perte cellulaire est plus rapide ou plus importante que le renouvellement des tissus, une dégénérescence du tissu et une perte progressive de fonction se mettent en place, conduisant à l’apparition de maladies (figure 3 : cas 2). Par exemple, une perte cellulaire au niveau du pancréas va progressivement conduire à une production d’insuline insuffisante ne permettant plus de réguler la glycémie, c’est-à-dire le taux de sucre dans le sang, conduisant à la l’apparition d’un diabète.
Figure 3 : le maintien en santé représente l’équilibre entre la perte cellulaire et le renouvellement cellulaire. Si la perte cellulaire est plus importante que le renouvellement des tissus, une dégénérescence du tissu et une perte progressive de fonction se mettent en place, conduisant à l’apparition de maladies.
Par conséquent, soutenir le rôle naturel des cellules souches permet d’aider celui-ci à se maintenir en santé.
Références
Drapeau C., Le pouvoir insoupçonné des cellules souches, 2010, Les Editions de l’Homme.
Drapeau C., Eufemio G., Mazzoni P., Roth G. D., Strandberg S., 2012,. The Therapeutic Potential of Stimulating Endogenous Stem Cell Mobilization, Tissue Regeneration – From Basic Biology to Clinical Application, Prof. Jamie Davies (Ed.), ISBN: 978-953-51-0387-5.
Jang Y.Y., Collector M.I., Baylin S.B., Diehl A.M., Sharkis S.J., 2004, Hematopoietic stem cells convert into liver cells within days without fusion, Nat Cell Biol, 6(6):532-9.
Jensen G.S. and Drapeau C., 2002, The use of in situ bone marrow stem cells for the treatment of various degenerative diseases. Medical Hypotheses 59(4):422-8.
Leone A.M., Rutella S., Bonanno G., et al., 2006, Endogenous G-CSF and CD34+ cell mobilization after acute myocardial infarction. Int. J Cardiol. 111(2):202-8.
Mezey E., Chandross K.J., Harta G., Maki R.A., McKercher S.R., 2000, Turning blood into brain: cells bearing neuronal antigens generated in vivo from bone marrow, Science.;290(5497):1779-82.
Orlic D., Kajstura J., Chimenti S., Limana F., Jakoniuk I., Quaini F., Nadal-Ginard B., Bodine D.M., Leri A., Anversa P.,2001, Mobilized bone marrow cells repair the infarcted heart, improving function and survival. Proc Natl Acad Sci U S A. 98(18):10344-9.
Swenson E.S., Kuwahara R., et al., 2008, Physiological variations of stem cell factor and stromal-derived factor 1 in murine models of liver injury and regeneration, Liver Int 28(3): 308-18.
Tsai N.W. et al., 2014, The association between circulating endothelial progenitor cells and outcome in different subtypes of acute ischemic stroke, Clinica Chimica Acta 427: 6–10
Voltarelli J.C., Couri C.E.B., Stracieri A.B.P.L., Oliveira M.C., Moraes D.A., Pieroni F., Coutinho M., Malmegrim K.C.R., Foss-Freitas M.C., Simoes B.P., Foss M.C., Squiers E., and Burt R.K., 2007, Autologous nonmyeloablative hematopoietic stem cell transplantation in newly diagnosed Type 1 diabetes mellitus. JAMA. 297(14):1568-1576.
Werner N., Kosiol S., Schiegl T., et al., 2005, Circulating endothelial progenitor cells and cardiovascular outcomes. N. Engl. J Med. 353(10):999-1007.